
英语原文共 9 页,剩余内容已隐藏,支付完成后下载完整资料
高能密度锂硫电池阴极的新方法
概论:
替换内燃机或减少其使用的目标对于社会来说是一个棘手的问题。 目前的锂离子电池技术为这个问题提供了解决思路。 然而,其理论重量容量(〜300mA h g -1)太低,不能克服电动车辆中能量供应问题,并且它们的成本太高,不能维持电气化运输的商业可行性。 硫是最有前途的下一代阴极材料之一。 自20世纪60年代以来,研究人员已经研究了硫作为电池阴极的可行性,但是最近才在制备可商业使用的活性复合材料方面取得了巨大进步。 硫单质是在地球上大量存在的元素,作为阴极形成的锂硫电池体系与现有锂离子电池相比具有高达五倍的能量密度
在过去几年中,研究人员已经更接近解决与硫阴极相关的问题。研究人员成功地将绝缘的硫单质与碳或导电聚合物复合,增强其导电性,这些导电主体也能够对还原/氧化反应形成可溶性多硫化锂进行包封,抑制活性硫物质散失。这些可溶性放电产物的流失扩散是Li -S电池的关键问题,需要对其进行限域以便增加循环寿命和容量保留。使用介孔碳和具有多孔碳中空球的特殊结构设计已经做到超过100个循环的放电容量大于900mAh g -1的高度稳定放电。在抑制聚硫化物的溶解扩散问题中,聚合物包裹的碳/硫复合材料显示出了很好地稳定性(〜90%的初始容量保留)。同时添加剂也在硫电极设计中发挥了重要作用。例如,通过添加小部分(gt; 3wt%)的多孔二氧化硅或二氧化钛有效地充当多硫化物储库,降低它们在电解质中的溶解程度能够有效提高硫的利用率以及电池比容量。
1.介绍
在未来25年,能源需求将从目前的使用增加至少35%,而化石燃料的消费量将增长,而不是下降。 这将对世界不可再生能源储备造成越来越大的压力,也将极大地影响气候问题。 电能存储系统可以允许间歇式可再生能量发电机(风力,太阳能,波浪)的更广泛使用并且减少用于运输的化石燃料的消耗。 常规锂离子(Li-ion)电池利用具有晶体结构的阴极,其具有电子和离子导电性,并且可以可逆地嵌入锂离子而不发生大的结构变化。目前的研究正在达到这些阴极的理论能量密度极限,无法满足我们在电/插电式混合动力车辆中的能量需求。因此必须引入能量密度更高的材料,而锂硫电池可以通过硫单质作为阴极通过氧化还原驱动作为电量储存体系,这一体系由于其使用无毒元素,高能量密度,以及成本低,环境友好等因素,在未来十分具有发展前景。
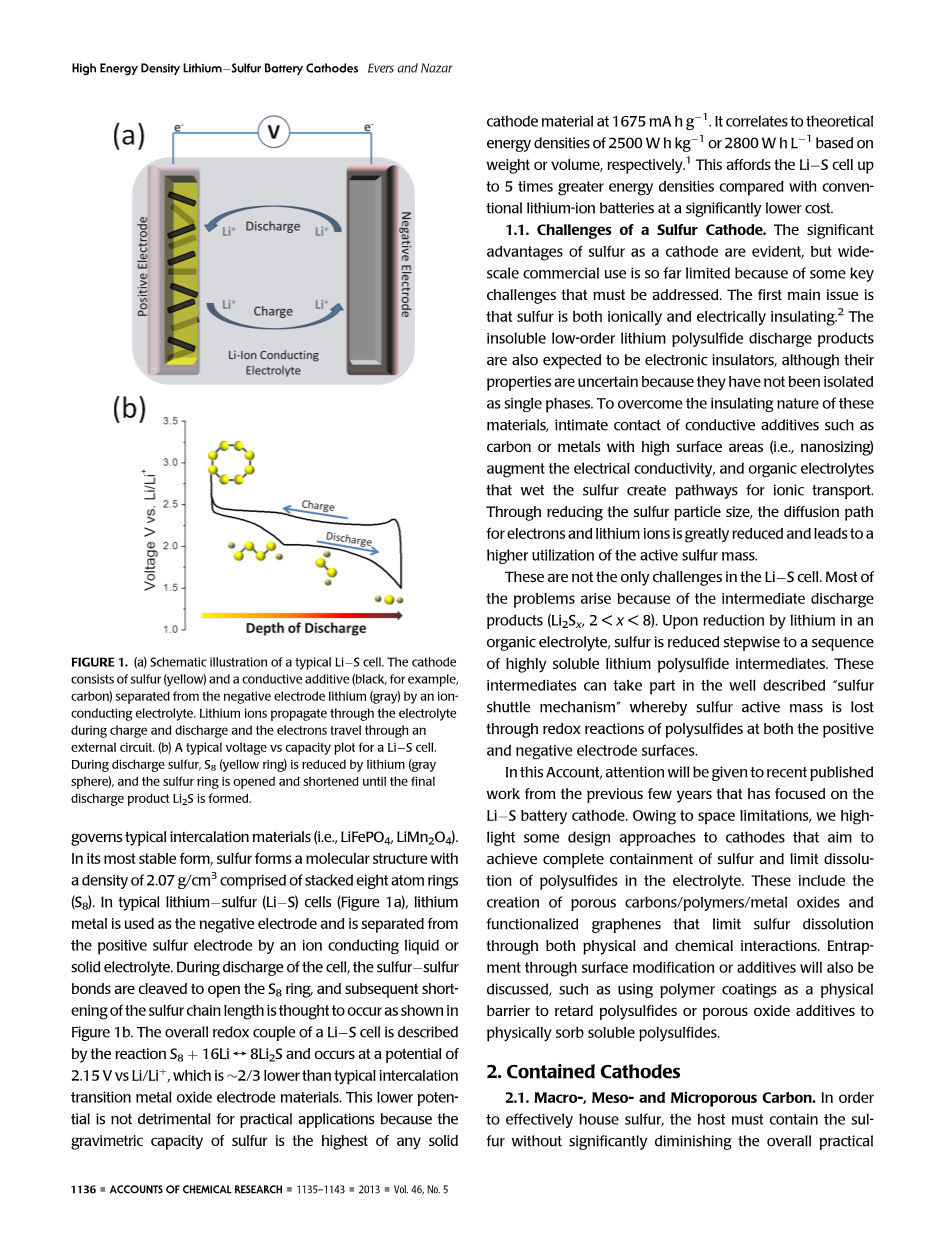
硫是锂电池的有希望的阴极,因为它的化学机理与典型的插层材料(即,LiFePO 4,LiMn 2 O 4)的嵌入脱出机理有着显着不同。在其最稳定的形式中,硫形成由堆叠的八个原子环(S8)组成的密度为2.07g / cm 3的分子结构。在典型的锂硫(Li 2 S)电池(图1a)中,锂金属作为负极,并通过电解液与隔膜或固体电解质与正硫电极分离。在电池放电期间,硫硫键断裂以打开S8环,形成短链的硫,如图1b所示。 Li - S电池的总体氧化还原反应可以表示为:S8 16Li8Li2S,并发生在2.15V相对于 典型的插层过渡金属氧化物电极材料Li / Li 的电位要低2/3。但这种较低的电势对于实际应用并不是有害的,因为硫的比容量为1675mA h g -1比任何固体材料都要高。 其理论能量密度达到2500Wh kg -1或2800Wh L -1,在成本更低的情况下达到了常规锂离子电池5倍的能量密度[1]。
图1.(a)典型Li - S电池的示意图。 阴极由硫(黄色)和导电添加剂(黑色,例如,碳) 通过电解质与负极锂(灰色)进行离子传导。 在充放电过程中,锂离子通过电解液传播,电子通过外电路传递。
(b)Li - S电池的典型充放电平台图。在放电硫期间,S8(黄色环)被锂还原(灰色球体),并且硫环被打开和缩短直到最终形成放电产物Li 2 S.
1.1硫阴极面临的挑战
硫作为阴极具有许多的优点,但是由于一些关键问题亟待解决,难以实现大规模商业使用。 第一个主要问题是硫是离子和电绝缘的[2],不溶性低级多硫化锂放电产物也是电子绝缘体,而且由于各种产物未被隔离成单相,导致性质的不确定性。 为了克服这些材料的绝缘性质,通过使用高表面积(即纳米级)的导电添加剂如碳或金属与其紧密接触来增强导电性,并且有机电解质通过浸润硫单质产生了用于离子传输的路径。 通过减小硫颗粒尺寸,电子和锂离子的扩散路径被大大降低,使活性硫质量得到更高的利用率。
这些不是Li-S电池中唯一的挑战。大多数问题是由于中间放电产物(Li 2 S x,2 lt;x lt;8)而产生。 在有机电解质中被锂还原时,硫逐步降低为一系列高度可溶的多硫化锂中间体。 这些中间体会发生“穿梭效应”,并且硫活性物质会通过多硫化物在正极和负极表面的氧化还原反应而损失。
因此,我们侧重回顾了过去几年,基于Li-S电池阴极的一些研究工作。 由于篇幅限制,我们侧重强调了一些阴极的设计方法,其目的皆在于实现完全容纳硫并限制多硫化物在电解质中的溶解问题。其中包括了通过物理和化学相互作用限制硫溶解的多孔碳/聚合物/金属氧化物和官能团修饰的石墨烯。本文也将讨论通过表面改性或添加剂对于活性硫的限制作用,例如使用聚合物包裹作为物理屏障以阻碍多硫化物流失,或通过多孔氧化物添加剂对可溶性多硫化物进行物理吸附。
2.阴极载体材料
2.1.大孔、介孔、微孔碳材料
为了有效地担载硫,主体材料必须在载硫的同时不显著的减少电池的总体性能,即重量/体积能量密度。 满足这些条件的最佳材料是轻质的,导电的,并且可以与绝缘硫形成导电结构,例如碳材料担载硫。 这种结构在最早的报告中有所提及,但是由于原始碳结构,它不能通过捕获硫及其还原物质来限制多硫化物的溶解。
碳作为电子良导体,保证了硫的氧化还原反应的可行性,同时他也可以作为骨架材料对氧化还原产物进行限域。 直接的解决方案是在载硫碳材料中引入孔。 孔径由IUPAC定义为大孔(gt; 50nm),介孔(2le;50nm)和微孔(lt;2nm)。 这些孔碳材料及其组合材料在过去2年中已经应用于实验,表现出不同的效应。
大孔碳由于它们的开放结构因此很少被用于Li -S电池,大孔对于抑制可溶性多硫化物溶解是无效的。然而,如果大孔碳耦合到高粘度电解质,多硫化锂的迁移率受到限制,将主要保留在阴极处。渡边等人使用有序的反蛋白石碳来容纳硫并且用高粘度的甘醇二磷酸盐代替常用的低粘度有机电解质[3]。该电解质类似于室温离子液体,因为其仅由[Li(glyme)] 阳离子和TFSI-阴离子构成。它提供了较稳定的充放电循环,在50个循环后具有超过700mAh g -1的可逆容量,和97%的库伦效率。 尽管结果是可观的,但是由于电流密度低(139mA g -1),反蛋白石碳难以大规模制备导致大规模应用是有问题的。
最近报道的大多数关于多孔碳阴极材料的研究集中在介孔碳(MCs)上,在我们小组的早期工作中,以小介孔碳(3〜4nm)载硫并以亲水性聚合物包覆有效的限制了硫及其还原产物的流失,产生高达1320mA hg-1的高可逆容量[4]。由此涉及一个问题:什么孔径及其分布是最佳的。刘等人已经使用系统的方法来确定孔径和硫负载对Li - S电池的循环稳定性和总容量的影响[5]。使用硬模板方法合成具有可调孔径(3,7,12和22nm)的一系列MC s并且孔体积高达〜4.8cm 3 / g,再使用两步法以不同的重量比将硫渗透到各种MC中,将溶解在CS2中的硫与MC混合,干燥,将复合物在155℃加热,由于硫较低的黏度而流入孔道内。 硫的质量分数随着MC的孔径的增加而逐渐增加,并且对于22nm的MC材料有报道做到硫质量分数达到83%。令人惊讶的是,所有的硫/碳复合材料表现出几乎相同的初始硫利用率,即使在MC之间硫的质量分数有着显著不同(56-84wt%)。这表明即使MC完全“填充”了硫,也不会对电池性能产生影响。 具有最大孔径和体积的MC显然应当用于优化重量和体积容量。
硫捕获的另一种方法是利用双峰MC作为硫主体。 这个概念首先由达德尼等人使用分层结构的硫碳(S / C)纳米复合材料作为高表面积阴极[6]。通过软模板合成方法合成具有7.3nm的均匀分布的中孔的多孔碳,然后通过KOH活化导致具有小于2nm的微孔出现,同时保持原始碳的完整性。最近的工作使用双模板方法产生双峰碳,直接制造孔径分布在〜6和〜2nm孔之间的高度有序碳[7,8]。每个孔贡献相等量的孔体积且孔壁上存在更小的孔,当硫浸渍到碳主体中时,较小的孔优先首先被填充(图2a)。较大的孔促进电解质在整个结构中的溶解渗透,较小的孔对硫及其还原产物进行限域。纳萨尔等人通过在具有相同孔分布的尺寸上产生约300nm的球形双峰碳粒子(图2b),对该概念进行了改进,并且能够以1C的高电流下保持高且相对稳定的850mAh g -1比容量(图2c)[9]。
另一种类似于创建双峰孔结构的方法已经由阿彻等人进行了实验,合成出具有3nm孔径及200nm内腔直径的介孔空心碳球[10],虽然这在大多数方面可能不被认为是双峰的,但介孔中空碳壳能有效的限制住硫及其还原产物的流失。据报道,中空碳球载硫量能达到70%,并且以适中的C / 5速率在100个循环后,它们保留了其初始容量(1071mA h g -1)的91%。 中空碳球的缺点是多孔碳壳的脆性和该方法的可伸缩性。 对于硫蒸汽浸渍法,需要三次单独的步骤才得以获得高的硫负荷。
微孔碳也已经用作载体应用于Li -S电池中。加奥等人使用蔗糖作为碳前体以形成具有小于1nm的非常窄的孔径分布的微孔碳球[11]。它们的材料表现出高度稳定的循环,具有42%质量分数的硫负载和高于900mAh g -1的高容量。 然而,当硫含量增加到51%时将显着地降低放电容量至600mA h g -1。该材料还表现出不寻常的放电曲线,不具有大多数其他Li -S报告特征的两个电压平台。这可能是由于碳与硫的反应,由于热处理或为此工作选择的碳酸烷基酯电解质混合物而形成键合的C-S复合材料。阿布鲁纳等人研究显示碳酸酯基溶剂在亲核硫化物阴离子存在下会发生副反应[12]。奥尔巴克,戈萨奇等人将活性炭(纤维形式)作为硫的微孔主体进行了研究,并且未使用粘合剂[13]。廉价的商业AC布经碳化形成具有高表面积(2000m 2 / g)和窄孔径分布(lt;2nm)的碳材料,硫担载达到33%质量分数,并在150mA g-1的电流密度下循环。获得了具有非常高的库仑效率的比容量达到1057mAh g -1的大的,稳定的放电容量。后者通过在电解质中使用LiNO 3来钝化负极并限制硫穿梭效应。
图2.(a)双峰中孔碳的孔径分布(BMC)。
(b)球形的TEM显微照片,BMC纳米颗粒显示2-D六角结构。
(c)70%wt硫的BMC纳米颗粒以1C倍率循环的性能。
2.2石墨烯
可以说,这是过去十年中Li-S电池中最受欢迎的与硫复合的材料。石墨烯具有非常高的导电性,大的表面积以及通过表面官能化调节疏水性/亲和性的能力,使得有多种方法与硫复合制备有效电极[14-19]。已经采用了两种不同的设计用于制备硫/石墨烯复合材料,每种设计都有其积极的特性。第一种方法利用由石墨烯/石墨烯氧化物片包围大的硫颗粒,而不是利用聚合物层包覆[15]或硫颗粒简单地与石墨烯紧密接触[17,18]。通过一步法原位生长硫颗粒(图3a)能够得到质量分数在87%的复合材料,在C / 5倍率表现出相对稳定的循环[18]。使用类似的流程能够形成氧化石墨烯/硫复合材料,然后通过热处理步骤将硫熔融进入3D无序的GO片材[17]。该复合材料显示出极其稳定的循环,使用离子液体/ PEGDME电解质以C / 10倍率,在50个循环中仍具有950mA hg -1的可逆容量(图3b)。
结合硫和石墨烯的另一种方法是将硫颗粒夹在官能化的石墨烯片之间并施加聚合物涂层。由于全氟磺酸 SO3 -的排斥作用而来抑制阴极的硫损失[16]。热膨胀氧化石墨也是有效的3D网络; 我们注
剩余内容已隐藏,支付完成后下载完整资料
资料编号:[136673],资料为PDF文档或Word文档,PDF文档可免费转换为Word
您可能感兴趣的文章
- 二氧化钛纳米管的合成及气敏性能研究进展外文翻译资料
- 水泥水化过程中的核磁共振扩散与弛豫研究——一种阐明胶凝材料内部后固化机理的非破坏性方法外文翻译资料
- 硫酸盐侵蚀混凝土的困惑世界外文翻译资料
- 通过用高子价的调节在金属有机骨架中产生分层孔隙外文翻译资料
- 一种稳定的ZIF-8涂层网膜,具有微米/纳米结构,可通过简便的制造方法生产,用于高效油水分离外文翻译资料
- 通过金属有机框架合成蛋黄壳状磷掺杂的二硫化镍/碳用于 高性能钠离子电池外文翻译资料
- 单层CrI3的应变可调磁学性能和电学性能外文翻译资料
- 脱合金铂金铜电催化剂对氧还原和甲醇氧化反应的活性和 稳定性的改善外文翻译资料
- 关于不同的冷冻制度制备具有单向排列通道的 YSZ多 孔陶瓷在孔道尺寸控制上的研究外文翻译资料
- 以单晶VO2和聚(3,4-乙烯二氧噻吩)的超薄混合纳米带作为-种 高容量且高倍率的水系锌离子电池的阴极材料外文翻译资料


